Myeloid Targeting Platform™
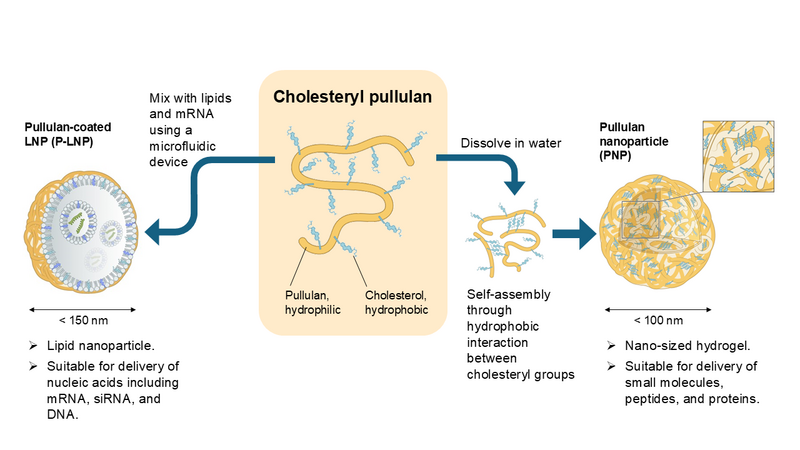
当社の Myeloid Targeting Platform™には現在、多糖プルランから成る2種類のナノ粒子、すなわち「プルランナノ粒子(PNP)」と「プルラン被覆(PEG不含)脂質ナノ粒子(P-LNP)」があります。PNP は低分子化合物、ペプチド、タンパク質の搭載と送達に適しています。P-LNP は mRNA、siRNA、DNAなどの核酸の搭載と送達に適しています。搭載する有効成分のタイプに応じてPNPまたはP-LNPのいずれかのナノ粒子を選択することで、多様な有効成分を疾患やワクチンに関連するミエロイド細胞、すなわちマクロファージや樹状細胞に選択的かつ効率良く送達できます。
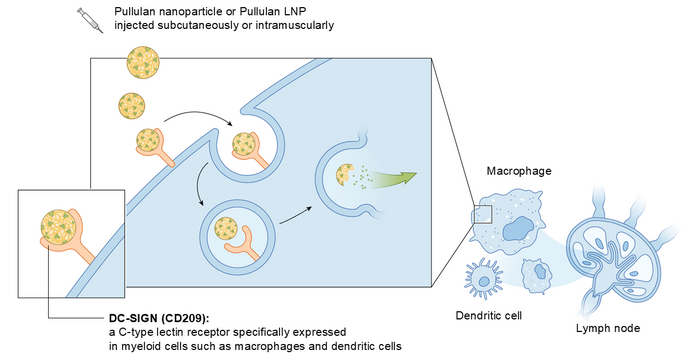
Myeloid Targeting Platform™がマクロファージや樹状細胞に薬剤を送達するメカニズムは、Myeloid Targeting Platform™に含まれる多糖プルランがこれらの細胞に発現する受容体蛋白「DC-SIGN(CD209)」に選択的に結合することに依ります。DC-SIGNを発現するミエロイド細胞はリンパ節などのリンパ器官のほか、がんなどの病変部に局在することが知られています。例えば多くの固形腫瘍には腫瘍関連マクロファージ(TAM)と呼ばれるマクロファージが豊富に存在します。TAMは強力な免疫抑制機能を発揮し、腫瘍の免疫逃避や治療抵抗性に寄与しています。TAMの多くがDC-SIGNを発現することが知られており、Myeloid Targeting Platform™を用いてDC-SIGNを通じて治療薬をTAMに送達し、これら細胞の機能を改変することで腫瘍の免疫逃避や治療抵抗性を解除することが可能と考えられます。
プルランナノ粒子(PNP)
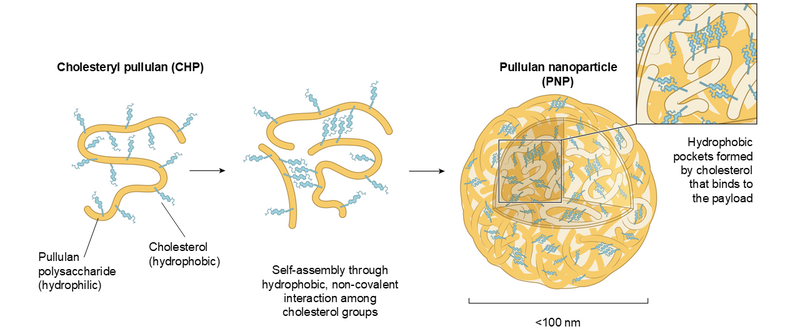
プルランナノ粒子(PNP)は、多糖プルランをコレステロールで修飾した「コレステロール修飾プルラン」が形成するナノ粒子です。プルランは微生物が生産する多糖で、生物学的に不活性で安全であり、化粧品や食品、医薬品の添加物に広く利用されています。PNPには疎水性低分子化合物、ペプチド、タンパク質(抗体フラグメントを含む)などの様々な有効成分を搭載できます。PNP は静脈内、皮下または筋肉内注射によって投与でき、病変部やリンパ器官に存在するDC-SIGN発現ミエロイド細胞(マクロファージや樹状細胞)に対し、PNPに搭載した有効成分を選択的に送達します。この選択的送達は、PNPが含む多糖プルランがミエロイド細胞に発現するDC-SIGNへ特異的に結合することによって達成されます (ウェブページへのリンク)。PNPの主な利点は以下の通りです。
DC-SIGNを発現し疾患やワクチンに関連するマクロファージおよび樹状細胞への有効成分やワクチンの選択的送達。
生物学的に不活性で高い安全性。
PNPには抗原性がなく複数回投与が可能。
シンプルな製造工程。
プルラン脂質ナノ粒子(P-LNP)
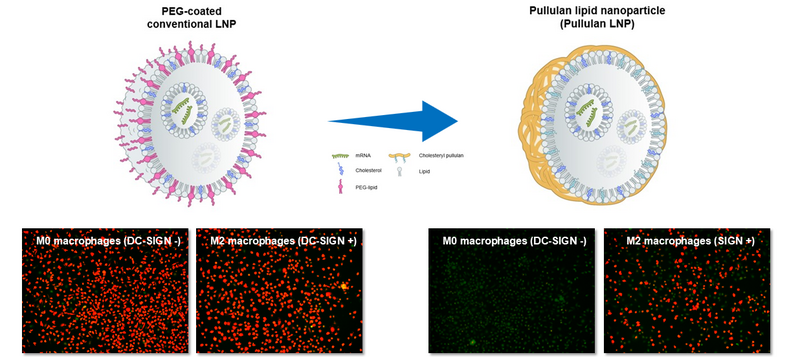
近年、脂質ナノ粒子(LNP)はがんや感染症に対する mRNA ワクチン、さらには RNA ベースの治療薬の開発において製薬業界での重要性が高まっています。現在のLNPには組織および細胞に対しての能動的な選択性(アクティブターゲティング能)がなく、高い薬剤濃度による副作用の可能性や、有効性が限定的となる可能性があります。またLNPは通常、ポリエチレン グリコール(PEG)を含みます。PEG は複数回投与すると抗 PEG 抗体を誘導し、アレルギーやアナフィラキシーなどの副作用を引き起こす可能性があります。また、抗PEG抗体は血液クリアランス促進(ABC)効果を引き起こす可能性があり、PEGを含むワクチンや薬剤の反復投与後に効果が低下するリスクがあります。
当社の Myeloid Targeting Platform™ の一つであるプルラン被覆LNP(P-LNP)は、樹状細胞やマクロファージなどの抗原提示細胞にDC-SIGN依存的に核酸医薬品成分を送達するPEG不含LNP を実現します。P-LNP は抗原性が低く複数回投与が可能で、ABC 効果やその他の PEG 関連の副作用のリスクを低下させる可能性があります。P-LNPはmRNA、siRNA, DNAなどの搭載と送達を得意とします。
ミエロイド細胞受容体「DC-SIGN」
プルラン ナノ粒子(PNP)およびプルラン被覆脂質ナノ粒子(P-LNP)のミエロイド細胞への標的化は、これらの細胞に発現する C 型レクチン受容体 DC-SIGN(別名CD209)への多糖プルランの特異的結合によって達成されます。 DC-SIGN は各種リンパ器官のマクロファージや樹状細胞、皮膚のランゲルハンス細胞、肝臓のクッパー細胞、脂肪組織のマクロファージなどの表面に存在します。 DC-SIGN の生理学的役割は病原体上の多糖類を感知し、細胞内への病原体の取り込みを促進することです。 DC-SIGN は抗原提示細胞とT 細胞のコンタクトも仲介します。
多くの固形腫瘍においては、DC-SIGN は主に腫瘍微小環境内で免疫抑制を促進する抗炎症性 のM2 様腫瘍関連マクロファージ(TAM)に発現します。 DC-SIGN の発現または M2 様 TAM の頻度は腫瘍の進行、予後不良、および免疫チェックポイント阻害薬に対する治療抵抗性に関連することが報告されています。このほか、多発性硬化症に関わるミクログリア細胞もDC-SIGNが発現するという報告があります。
当社の対象分野
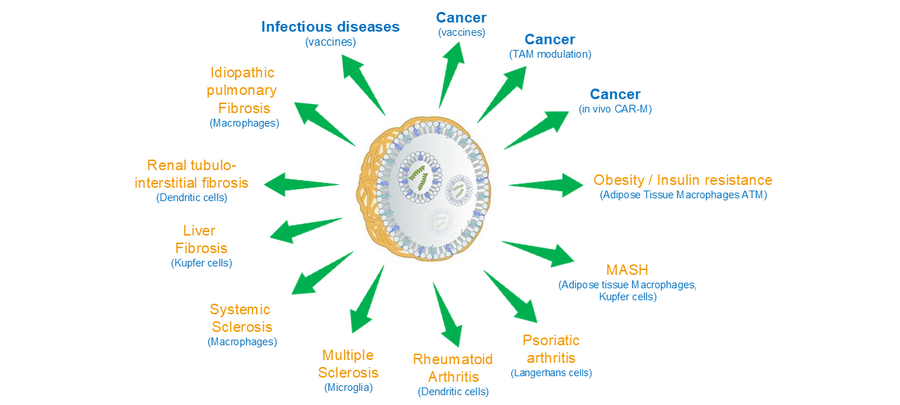
最近の研究では、マクロファージや樹状細胞ががん、線維症、ウイルス感染、炎症や神経変性疾患、代謝性疾患、自己免疫疾患などの多くの主要な疾患に直接関与していることが示されています。 ヒト固形腫瘍では肝臓がん、膀胱がん、腎細胞がん、胃がん、頭頸部がん、肺がんなどの多くの腫瘍タイプで DC-SIGN の発現が観察されます。これら疾患は当社の Myeloid Targeting Platform™を利用した新しい免疫療法の潜在的な適応症となります。
DC-SIGN の発現は特発性肺線維症(IPF)、腎尿細管間質性線維症、多発性硬化症、関節リウマチ、乾癬性関節炎、ウイルス感染症、肥満、非アルコール性脂肪肝疾患 (NAFLD)などでも報告されています。これらの疾患におけるDC-SIGN 発現ミエロイド細胞に対し、 PNPまたはP-LNP で治療薬を疾患局所に選択的送達することで有効性と安全性に優れた医薬品を創製できる可能性があります。
健常人ではDC-SIGN はリンパ節、皮膚、脾臓などの重要なリンパ器官に局在する樹状細胞に発現します。これらのミエロイド細胞はワクチン接種を行ったときの抗原提示と抗ウイルスまたは抗がん免疫応答の効率的な誘導において中心的な役割を果たしています。当社の Myeloid Targeting Platform™はリンパ器官のミエロイド細胞にワクチン抗原を効率的に送達するのに理想的であり、既に複数の臨床試験においてがんペプチド/タンパク質ワクチンにおけるワクチン送達システムとして安全性と治療効果を示唆する結果が報告されています。